PZ 24/12 Formoterol- oder Budesonid-Formoterol-haltige Pulverinhalatoren: Unterschiedliche Angaben der Wirkstoffstärke bei Importen
Information
Formoterol- oder Budesonid-Formoterol-haltige Pulverinhalatoren: Unterschiedliche Angaben der Wirkstoffstärke bei Importen
AMK / Die Arzneimittelkommission der Deutschen Apotheker (AMK) erhält in jüngster Zeit vermehrt Anfragen aus Apotheken zu importierten Formoterol- oder Budesonid-Formoterol-haltigen Pulverinhalatoren. Unterschiedliche Angaben zur Wirkstoffstärke bei ein und demselben Präparat haben zu Irritationen bei Patienten und in Fachkreisen geführt.
Um den Bestimmungen des Arzneimittelgesetzes zur Kennzeichnung von Fertigarzneimitteln (§ 10 AMG) nachzukommen, verwenden Importeure in der Praxis zumeist entsprechend bedruckte Aufkleber, die die ausländische Deklaration überdecken.
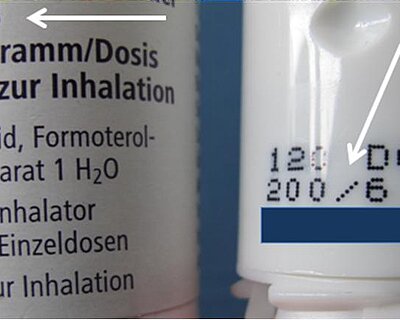
Bei Fertigarzneimitteln zur Inhalation können je nach EU-Mitgliedsstaat unterschiedliche Angaben zur Wirkstoffstärke üblich sein. So kann ein Budesonid-Formoterol-haltiger Pulverinhalator für den deutschen Markt mit einem Aufkleber, welcher beispielsweise mit der Wirkstoffstärke „160/4,5 µg“ bedruckt wurde, versehen sein. Diese Angabe bezieht sich in Deutschland üblicherweise auf die über das Mundstück abgegebene Wirkstoffmenge. Wird nun der Aufkleber oder die schützende Hülle vom Patienten entfernt, kann es zu Irritationen kommen, wenn dort eine andere Wirkstoffstärke wie „200/6 µg“ lesbar ist. Diese bezieht sich jedoch auf die im Behältnis abgemessene Wirkstoffmenge(siehe Foto).
Auf die unterschiedlichen Varianten der Angabe der Wirkstoffstärke bei Pulverinhalatoren in EU-Mitgliedsstaaten wird in den Fachinformationen der jeweiligen Importpräparate hingewiesen. So wird darin erläutert, dass die im Behältnis abgemessene Wirkstoffmenge (200/6 µg) der über das Mundstück abgegebenen Wirkstoffmenge (160/4,5 µg) entspricht.
Diese Informationen sollten eine angemessene Beratung der Patienten, bei denen Irritationen aufgetreten sind, ermöglichen. Die AMK bittet darum, bei weiteren Unklarheiten zu unterschiedlichen Angaben der Wirkstoffstärke importierter Pulverinhalatoren die Geschäftsstelle zu kontaktieren.